Navigation des services
Recherche
La petite bête que vous voyez ci-dessus – et qui répond au doux nom de Gerris lacustris – marche sur l’eau ! Elle n’est pas la seule, me direz-vous, mais c’est tout de même une performance remarquable. Quel est donc son secret ? Certes elle est très légère, mais ça n’explique pas tout !
Pour percer ce mystère, il est nécessaire de nous plonger (c’est le cas de le dire) dans la structure intime du plus merveilleux liquide inventé par la nature, alpha et oméga de toute vie sur Terre ainsi que de tout phénomène météorologique : l’eau.
Pour cela, il va falloir parler d’atomes et de molécules ! Non, ne partez pas ! Vous verrez, ce n’est pas si compliqué.
Structure moléculaire de l’eau
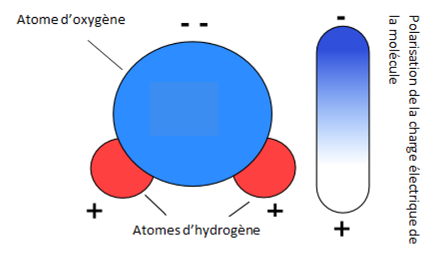
Une molécule d’eau est composée de 2 atomes d’hydrogène et d’un atome d’oxygène. Ces atomes pris séparément sont électriquement neutres car ils contiennent autant d’électrons (chargés négativement) que de protons (chargés positivement). Une molécule d’eau contient en tout 10 protons et 10 électrons ; or ces électrons - pourtant partagés entre les trois atomes - ne sont pas répartis également à l’intérieur de la molécule car l’atome d’oxygène leur fait une cour assidue et les attire majoritairement à lui. Dès lors, il se retrouve avec une charge négative, alors que les deux atomes d’hydrogène sont chargés positivement. On dit de la molécule d’eau qu’elle est « polarisée », raison pour laquelle elle se comporte comme un petit aimant, son côté positif étant attiré par le côté négatif de ses voisines et inversément.
Mécanisme de la tension superficielle de l’eau
Une molécule d’eau située, disons, au milieu d’un verre d’eau se retrouvera entourée d’autres molécules d’eau avec lesquelles elle se liera de tous côtés, chaque liaison lui coûtant un peu d’énergie. Etant attirée à la fois et de manière égale dans toutes les directions, cette molécule sera très stable au sein du liquide.
Les molécules d’eau situées en surface en revanche ne seront pratiquement pas attirées par les molécules d’air (azote, oxygène, vapeur d’eau) très peu denses situées au-dessus d’elles. Elles mettront donc toute leur énergie à se lier avec les molécules d’eau situées au-dessous, et surtout à côté d’elles. Moins nombreuses, ces liaisons seront en revanche plus fortes, plus difficiles à rompre, et conféreront à la surface de l’eau une plus grande cohésion, appelée « tension superficielle de surface ».
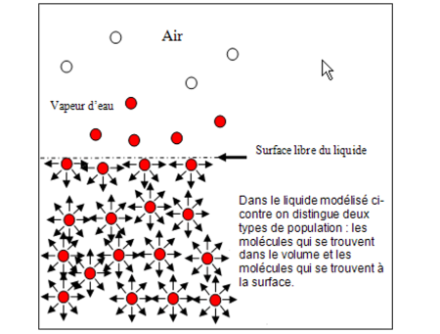
Les molécules d’eau situées à la marge d’un liquide (surface, goutte, etc…) agissent donc un peu comme une coquille plus ou moins rigide, ou un film de plastique. Ainsi s’expliquent les petites dépressions visibles sous les pattes du Gerris de la photo ouvrant cet article.
Le saviez-vous ?
Le poids maximal d’un objet pouvant être maintenu en suspension par la tension superficielle d’un liquide dépend de la force de cohésion des molécules dudit liquide. Ainsi, un liquide très dense pourra supporter des objets autrement plus lourds qu’un Gerris ou qu’un brin d’herbe.
Dans le processus de flottaison, le principal mécanisme à l'oeuvre reste toutefois - et de loin - la force d'Archimède, dont la loi peut être résumée ainsi : un objet flotte tant que le poids du liquide déplacé excède celui de l'objet. Cette condition est présente lorsque la masse volumique du liquide est supérieure à celui de l'objet (si celui-ci est massif) ou par exemple si l'objet est creux et que son volume contient beaucoup d'air. Ainsi, bien que composé de métal, un paquebot flotte car l'immense volume d'eau qu'il déplace pèse davantage que lui.

Pour conclure, mentionnons quand même que le Gerris Lacustris ne travaille pas sans filet et a plus d’un tour dans son sac. Pour assurer le coup, il a sous les pattes de longs poils enduits d’une cire hydrophobe (qui repousse l’eau) contribuant à ses remarquables performances.